امیدواری به یک فناوری نوین ویرایش ژن برای درمان بیماری های خونی
به گزارش تا بینهایت، محققان می گویند در حال حاضر آزمایشات بکارگیری فناوری نوین ویرایش ژن موسوم به کریسپر(CRISPR) برای درمان بیماری های خونی موثر نشان داده است، اما این روش درمانی بسیار گران است.
به گزارش خبرنگاران و به نقل از آی ای، بر اساس مطالعه ای که در مجله پزشکی نیوانگلند(New England) منتشر شده است، دستیابی به یک موفقیت جدید در فناوری ویرایش ژن کریسپر برای بیماران مبتلا به بیماری های خونی همزمان با نویدها و مسائل جدیدی همراه شده است.
محققان موسسه کریسپر تراپیوتیکس(CRISPR Therapeutics) آنزیمی برای برش دی.ان.ای مهندسی نموده اند که سلول های خون را مجبور به فراوری هموگلوبین بیشتر می نماید و به بیماران اجازه می دهد بدون درد و بدون احتیاج به تزریق و انتقال منظم خون زندگی نمایند.
با این حال، درمان با این روش می تواند میلیون ها دلار هزینه داشته باشد، به این معنی که تا زمانی که هزینه این نوع درمان به طور قابل توجهی کاهش پیدا نکند، بسیاری از افراد از آن محروم خواهند ماند.
محققان روی دو شرایط تمرکز کردند، بتا-تالاسمی و کم خونی داسی شکل. بیماری کم خونی داسی شکل بیش از 100 هزار سیاه پوست را تنها در ایالات متحده تحت تأثیر قرار داده است. این بیماری موجب سفت شدن سلول های قرمز خون و دادن یک شکل هلالی به آنها می شود و باعث درد شدید در بیماران مبتلا و افزایش خطر آسیب به اندام، سکته و سایر مسائل سلامتی می شود.
کم خونی داسی شکل یا کم خونی سلول های داسی شکل(Sickle cell anemia) یک بیماری ژنتیکی و یک اختلال خونی است که با هموگلوبین معیوب(Hbs) شناخته می شود. هموگلوبین طبیعی صاف و گرد است و به سلول اجازه عبور آسان از مویرگ های خونی را می دهد. سلول های هموگلوبین سلول داسی سفت و به شکل داس می باشند. این سلول ها تمایل دارند به شکل خوشه ای و در کنار یکدیگر قرار گیرند، بنابراین به راحتی از مویرگ های خونی عبور نمی نمایند. این خوشه ها به توقف جریان خون حمل نماینده اکسیژن منجر می گردند. برخلاف سلول ها با هموگلوبین طبیعی که بیش از 120 روز زنده هستند، سلول های داسی بعد از 10 تا 20 روز از بین می فرایند. این فرایند طی یک دوره مزمن منجر به بروز کم خونی می شود. کم خونی داسی شکل حاصل یک جهش ژنی است.
اکنون این روش درمانی جدید، یک درمان عالی است، اما به دلیل گران بودن، مشکل جهانی این بیماری را حل نمی نماید. بیماران در موارد شدید ابتلا، پیوند مغز استخوان انجام می دهند که یک درمان پرخطر است و احتیاج به اهدا نمایندگان کاملاً همسان دارد که یافتن آن نیز بسیار سخت است.
در حالی که درمان کریسپر به پیوند مغز استخوان نیز احتیاج دارد، اما از سلول های بنیادی خون خود بیمار استفاده می شود.
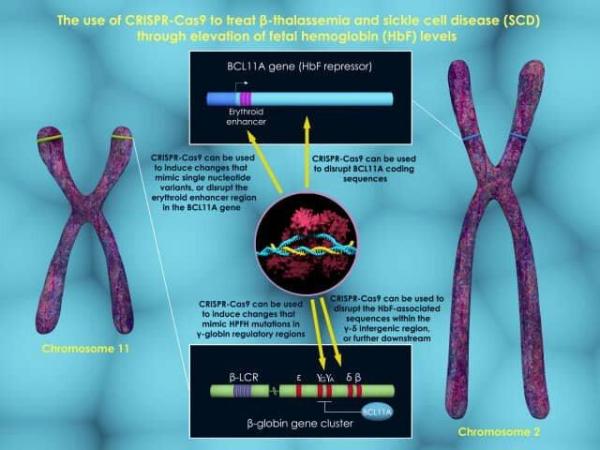
ابتدا سلول های بنیادی خون از بیمار استخراج شده و سلول های معیوب با استفاده از شیمی درمانی درست مثل پیوندهای منظم مغز استخوان نابود می شوند. سپس، محققان از آنزیم برش دهنده دی.ان.ای کریسپر و راهنمایی آر ان ای برای شکستن BCL11A -یک سوئیچ ژنتیکی که ژن هموگلوبین جنین را در اوایل زندگی شخص خاموش می نماید- استفاده کردند.
با فعال شدن مجدد آن ژن، هموگلوبین جنینی فراوری می شود که هموبلاگین از دست رفته بیماران بتا-تالاسمی را بازیابی می نماید و هموگلوبین معیوب را در بیماران کم خونی داسی شکل جایگزین می نماید. در نتیجه، بیشتر بیماران در این آزمایشات مقدار کافی هموگلوبین جنینی ایجاد کردند و دیگر احتیاجی به انتقال خون نداشتند.
محققان برای اطمینان از عدم وجود هیچ عارضه جانبی مانند سرطان که می تواند ناشی از کریسپر باشد، باید مدت طولانی تری بیماران را پیگیری نمایند. با این حال، بزرگترین مسئله هنوز هزینه این درمان است. اگرچه محققان به طور دقیق به هزینه این درمان اشاره نکردند، اما تخمین زده شده است که چنین روشی برای هر بیمار 1.8 میلیون دلار هزینه داشته باشد که شامل شیمی درمانی و بستری در بیمارستان نیز هست.
با این حال، موسسه ملی بهداشت آمریکا و بنیاد خیریه بیل و ملیندا گیتس به امید کاهش هزینه های چنین روش هایی تا چند صد میلیون دلار به توسعه این فناوری تزریق می نمایند که می تواند شامل روش های درمانی جدیدی باشد که احتیاج به پیوند مغز استخوان را از بین می برند.
منبع: خبرگزاری ایسنا